Ikatan logam merupakan salah satu jenis ikatan kimia yang terjadi pada unsur-unsur logam. Sifat-sifat fisik logam seperti kekuatan, konduktivitas listrik dan panas yang tinggi, serta kemampuannya untuk dibentuk menjadi lembaran atau kawat (malleabilitas dan duktilitas) disebabkan oleh adanya ikatan logam ini. Namun, apa sebenarnya yang dimaksud dengan ikatan logam? Bagaimana ikatan ini terbentuk, dan apa saja sifat serta aplikasinya dalam kehidupan sehari-hari?
Pada artikel ini, kita akan membahas pengertian ikatan logam, bagaimana mekanismenya, serta sifat-sifat fisik yang dihasilkan oleh ikatan ini.
1. Pengertian Ikatan Logam
Ikatan logam adalah jenis ikatan kimia yang terbentuk antara atom-atom logam. Ikatan ini terjadi ketika elektron-elektron valensi dari atom-atom logam dilepaskan dan membentuk lautan elektron yang bergerak bebas di antara ion-ion logam positif. Elektron-elektron ini tidak terikat pada satu atom tertentu, tetapi bergerak secara bebas di seluruh struktur logam, menciptakan sifat logam yang khas.
Dengan kata lain, ikatan logam melibatkan delokalisasi elektron, yaitu kondisi di mana elektron valensi tidak terikat pada satu atom, tetapi tersebar dan berbagi di antara banyak atom dalam kisi logam. Ini berbeda dengan ikatan ionik atau kovalen, di mana elektron dipertukarkan atau dibagi secara spesifik antara dua atom.
Contoh:
Logam seperti tembaga (Cu), besi (Fe), dan emas (Au) semuanya membentuk ikatan logam. Atom-atom logam ini berikatan kuat satu sama lain melalui lautan elektron, yang membuat logam memiliki struktur yang kokoh dan stabil.
2. Mekanisme Terbentuknya Ikatan Logam
Dalam ikatan logam, atom-atom logam cenderung memiliki elektron valensi yang sedikit, biasanya antara satu hingga tiga elektron pada kulit terluarnya. Karena gaya tarik antara inti atom dan elektron valensi ini relatif lemah, elektron-elektron tersebut dengan mudah “terlepas” dari atom inti. Ketika elektron valensi dilepaskan, mereka tidak lagi terikat pada atom individual, melainkan membentuk lautan elektron yang bergerak bebas di seluruh kisi logam.
Pada saat yang sama, inti atom logam yang bermuatan positif (karena kehilangan elektron) tersusun dalam pola tertentu, menciptakan struktur kisi kristal logam. Elektron-elektron yang bergerak bebas ini kemudian bertindak sebagai “lem” yang menahan atom-atom logam bersama dalam struktur yang padat.
Mekanisme Dasar Ikatan Logam:
- Delokalisasi Elektron: Elektron valensi dari atom-atom logam dilepaskan dan tersebar secara bebas di antara ion-ion logam.
- Interaksi Antara Ion Logam Positif dan Lautan Elektron: Ion-ion logam positif ditahan bersama oleh lautan elektron yang terdelokalisasi, yang memberikan stabilitas pada struktur logam.
3. Sifat-Sifat Fisik Logam yang Disebabkan oleh Ikatan Logam
Ikatan logam bertanggung jawab atas berbagai sifat fisik yang khas pada logam. Berikut beberapa sifat fisik utama logam yang terkait dengan adanya ikatan logam:
a. Konduktivitas Listrik dan Panas
Salah satu sifat paling menonjol dari logam adalah kemampuannya untuk menghantarkan listrik dan panas. Hal ini terjadi karena elektron bebas dalam logam. Elektron-elektron ini dapat bergerak dengan mudah ketika diberikan tegangan listrik, memungkinkan logam untuk menghantarkan listrik dengan sangat baik.
- Konduktivitas listrik: Saat tegangan listrik diterapkan pada logam, elektron-elektron bergerak dari daerah dengan potensial lebih rendah ke daerah dengan potensial lebih tinggi, yang menghasilkan aliran listrik.
- Konduktivitas panas: Elektron bebas juga memungkinkan logam untuk menghantarkan panas. Ketika bagian dari logam dipanaskan, energi kinetik dari elektron-elektron tersebut meningkat dan dengan cepat ditransfer ke seluruh bagian logam.
b. Kekuatan dan Kekerasan
Logam umumnya dikenal kuat dan keras karena struktur kisi kristalnya yang diikat oleh lautan elektron yang terdelokalisasi. Ikatan ini memberikan stabilitas tinggi, sehingga sulit bagi atom-atom logam untuk terpisah.
- Kekuatan tarik tinggi: Logam, seperti besi atau baja, memiliki kekuatan tarik yang tinggi, yang membuatnya tahan terhadap gaya yang menariknya memanjang.
- Kekerasan: Beberapa logam, seperti baja, dikenal karena kekerasannya, yang membuatnya tahan terhadap goresan dan deformasi.
c. Malleabilitas dan Duktilitas
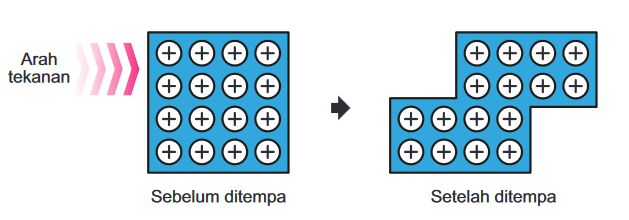
Logam bisa ditempa (malleable) dan dapat ditarik menjadi kawat (ductile) tanpa mudah patah. Hal ini disebabkan oleh kemampuan atom-atom logam untuk bergeser tanpa merusak struktur keseluruhan karena lautan elektron tetap menjaga ikatan antar atom.
- Malleabilitas: Logam dapat ditempa menjadi lembaran tipis melalui penempaan atau penekanan.
- Duktilitas: Logam dapat ditarik menjadi kawat tipis tanpa putus.
d. Kilau (Luster)
Logam memiliki permukaan yang mengkilap karena elektron bebas yang dapat menyerap dan memantulkan cahaya. Inilah yang membuat logam seperti emas, perak, dan tembaga tampak berkilau.
4. Contoh-Contoh Logam dan Penggunaan Ikatan Logam dalam Kehidupan Sehari-Hari
Ikatan logam memainkan peran kunci dalam berbagai aplikasi teknologi dan industri. Berikut beberapa contoh logam dan penggunaannya yang memanfaatkan sifat-sifat ikatan logam:
a. Tembaga (Cu)
Tembaga adalah logam yang sangat baik dalam menghantarkan listrik dan panas. Karena sifat konduktivitas listriknya yang luar biasa, tembaga digunakan secara luas dalam kabel listrik, peralatan elektronik, serta komponen listrik lainnya. Selain itu, karena sifat malleabilitasnya, tembaga juga mudah dibentuk dan digunakan dalam pembuatan pipa.
b. Besi (Fe) dan Baja
Besi, terutama dalam bentuk paduannya yang dikenal sebagai baja, digunakan dalam konstruksi bangunan, jembatan, serta peralatan mesin. Baja dikenal karena kekuatannya yang sangat tinggi, yang berasal dari ikatan logamnya yang kuat.
c. Aluminium (Al)
Aluminium adalah logam yang ringan namun kuat. Sifat konduktivitas panas dan daya tahannya yang baik membuatnya ideal untuk penggunaan di industri penerbangan, mobil, dan produk rumah tangga seperti kaleng dan panci.
d. Emas (Au) dan Perak (Ag)
Emas dan perak dikenal karena konduktivitas listrik yang tinggi dan tahan terhadap korosi. Karena itu, selain digunakan untuk perhiasan, emas dan perak sering digunakan dalam komponen elektronik presisi tinggi, seperti chip komputer dan sirkuit elektronik.
5. Kesimpulan
Ikatan logam adalah jenis ikatan yang melibatkan delokalisasi elektron di antara ion-ion logam positif. Proses ini memberikan logam berbagai sifat fisik unik seperti konduktivitas listrik dan panas, kekuatan, kilau, serta kemampuan untuk ditempa dan ditarik. Logam, melalui ikatan logamnya, memainkan peran penting dalam teknologi modern dan kehidupan sehari-hari, dari konstruksi bangunan hingga peralatan elektronik.
Dengan memahami sifat-sifat ikatan logam, kita bisa lebih mengapresiasi penggunaan logam dalam berbagai aspek kehidupan, serta teknologi yang berkembang pesat di sekitar kita.